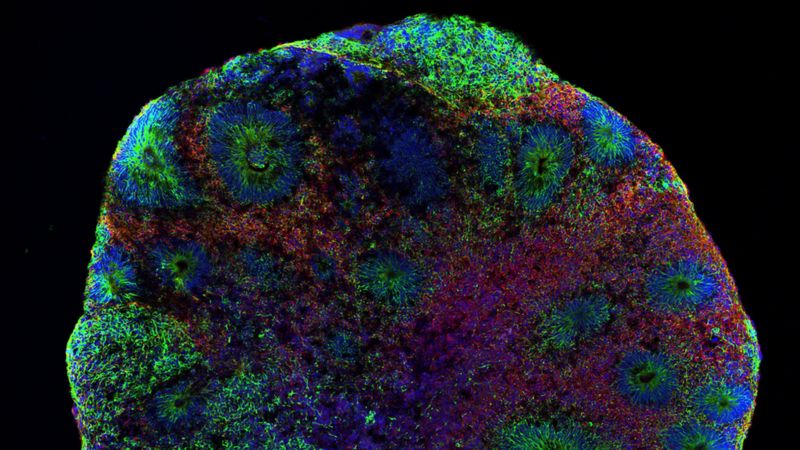
Imagine pegar um punhado de células humanas de diferentes tipos e, após uma série de procedimentos, transformá-las num órgão em miniatura, que funciona de verdade e pode ser observado a olho nu.
Saiba que isso já é possível nos dias de hoje: os miniórgãos (ou organoides, nome preferido entre os cientistas) são uma ferramenta poderosa, que ajuda a entender como o Sars-CoV-2, o coronavírus responsável pela pandemia atual, provoca danos em diferentes partes do nosso corpo.
Graças a essa tecnologia, os especialistas avaliaram diversos tratamentos possíveis e entenderam rapidamente que a covid-19 não era apenas uma doença que atingia o sistema respiratório, mas tinha repercussões no coração, no intestino, nos rins e até no cérebro.
Mas, afinal, como se cria um miniórgão? E quais as vantagens que ele traz em comparação com outros métodos mais antigos, como culturas de células e cobaias?
Voltar ao passado para projetar o futuro
A matéria-prima básica para a construção de um organoide são células simples presentes na pele ou no sistema urinário. Após a seleção, os cientistas realizam um procedimento que faz essas unidades se transformarem em células-tronco.
“É como se elas voltassem no tempo. Por meio de uma transformação genética, elas viram células-tronco novamente”, reforça a neurocientista Marília Zaluar Guimarães, do Instituto D’Or de Pesquisa e Ensino, no Rio de Janeiro (IDor).
A descrição desse processo biológico e da tecnologia capaz de torná-lo factível, inclusive, renderam o Prêmio Nobel de Medicina e Fisiologia de 2012 ao britânico John Gurdon e ao japonês Shinya Yamanaka.
Mas essa é apenas uma parte da história. Depois que as células “voltam no tempo”, é preciso realizar uma nova etapa. “De acordo com fatores que usamos no laboratório, fazemos com que essas células-tronco se diferenciem e se especializem novamente”, completa Guimarães, que também é professora na Universidade Federal do Rio de Janeiro (UFRJ).
Em outras palavras, é possível pegar uma célula da pele e, seguindo alguns passos, fazer uma metamorfose para que ela vire um neurônio ou um glóbulo vermelho.
A grande sacada é que os organoides não são apenas um amontoado de células que podem ser analisados com o auxílio de um microscópio. Falamos aqui de formações mais complexas, que reúnem mais de um tipo de célula e muitas vezes são visíveis a olho nu. Trata-se realmente de um órgão em escala reduzida.
“No caso dos minicérebros, por exemplo, eles são esféricos, mas não têm a mesma formação do órgão verdadeiro. O que nos permite saber que aquela estrutura se assemelha ao original são suas características celulares e bioquímicas”, aponta o biólogo Daniel Martins de Souza, da Universidade Estadual de Campinas (Unicamp).
As origens
Numa perspectiva histórica, a possibilidade de construir miniórgãos é muito recente. Os cientistas só conseguiram botar a mão na massa de verdade nos últimos dez anos.
Apesar de jovens, os organoides já deram grandes contribuições à ciência. Um dos maiores exemplos disso aconteceu durante a epidemia de zika, que preocupou o Brasil (e o mundo) em 2015 e 2016.
Transmitido por uma picada do mosquito Aedes aegypti, o vírus provoca sintomas relativamente simples, como febre baixa, dor e vermelhidão nos olhos.
Mas a explosão de casos de microcefalia (quando o bebê nasce com o crânio e o cérebro menores do que o usual) na região Nordeste do país levantou o sinal de alerta: será que uma infecção por zika ao longo da gravidez poderia estar relacionada a essa grave complicação?
A suspeita foi confirmada graças às pesquisas com os organoides. Em laboratório, uma equipe liderada pelo neurocientista Stevens Rehen, da UFRJ e do IDor, utilizou minicérebros para demonstrar que o zika realmente afeta células do sistema nervoso e inibe seu crescimento, ocasionando a síndrome congênita associada à infecção pelo vírus, que causou a microcefalia e diversos outros problemas de saúde em bebês.
“Essa foi a primeira vez que o modelo dos organoides foi utilizado para entender uma doença viral”, lembra Guimarães.
As vantagens
Nas últimas décadas, culturas de células e cobaias foram os principais meios para realizar os estudos preliminares com candidatos a remédios ou vacinas. A proposta estava em entender como essas novas moléculas agem numa escala menor e mais controlada antes de partir para os testes clínicos, que envolvem seres humanos.
Essas metodologias também permitem compreender como determinada doença afeta o organismo, mesmo que de maneira simplificada.
Mas as alternativas mais antigas trazem uma série de limitações, a começar por sua própria simplicidade, que não reproduz as mesmas características da vida real. “Os organoides, por outro lado, são compostos de diferentes células e têm uma estrutura tridimensional. Por isso, eles têm funções mais parecidas ao que acontece de verdade”, compara o farmacêutico Kazuo Takayama, professor da Universidade de Kyoto, no Japão.
No caso das cobaias, há ainda uma limitação na quantidade de animais disponíveis para uso em experimentos. “É possível cultivar miniórgãos em laboratório quase que infinitamente, então eles podem ser usados para testes com novos medicamentos em larga escala”, completa Takayama.
Conhecimento otimizado
Durante uma pandemia como a que vivemos, essa abordagem moderna também possibilitou acelerar alguns processos e obter informações essenciais com agilidade.
Sem os organoides, o conhecimento sobre a covid-19 demoraria muito mais para ficar disponível. Isso, por sua vez, impediria o avanço da ciência e atrasaria ainda mais a chegada de métodos de diagnóstico, prevenção e tratamento seguros e eficazes.
Vamos a exemplos práticos de como isso ocorreu durante os últimos meses. Diante da emergência sanitária global, muitos especialistas foram avaliar se existia alguma droga já disponível no mercado que poderia combater o vírus ou amenizar seu estrago.
Muitas dessas terapias foram testadas nos organoides. Aquelas que não funcionaram logo de cara foram descartadas. Os remédios que mostraram algum efeito inicial puderam, então, evoluir mais rápido para as próximas fases de pesquisa. Imagina quanto tempo foi economizado com essa triagem inicial?
Mas as aplicações vão muito além da área farmacêutica. Trabalhos feitos no Japão e nos Estados Unidos focaram em minipulmões e descobriram que o Sars-CoV-2 invade e destrói algumas células do sistema respiratório. Isso, por sua vez, pode gerar uma resposta inflamatória muito forte e danosa à própria saúde da pessoa acometida pela infecção.
“De forma geral, os organoides permitiram que entendêssemos que células humanas o coronavírus consegue invadir e usar para se replicar. Nosso grupo demonstrou que isso acontece no intestino, o que ajuda a explicar os sintomas gastrointestinais observados em muitos pacientes”, relatam os pesquisadores Joep Beumer e Maarten Geurts, do Instituto Hubrecht, na Holanda.
Outra experiência realizada na Universidade da Colúmbia Britânica, no Canadá, e no Instituto de Biotecnologia Molecular de Viena, na Áustria, construiu vasos sanguíneos em miniatura. A partir daí, foi possível observar que o vírus da covid-19 invade o endotélio (a camada interna de veias e artérias).
Isso tem duas implicações principais. A primeira é a formação de coágulos que bloqueiam a passagem de sangue e podem dar início a infarto, AVC ou trombose. Em segundo lugar, há a suspeita de que, a partir da circulação, o patógeno consegue “vazar” para diversas áreas do corpo e afetar outros órgãos importantes.
As iniciativas não param por aí: nessa mesma linha, trabalhos com organoides continuam a avaliar as pegadas do coronavírus no fígado, nos rins, no coração e no cérebro.
Atuação nacional
No Brasil, dois grupos de pesquisa se debruçam sobre as repercussões da covid-19 no cérebro humano. No IDor, os cientistas utilizaram neuroesferas (um tipo mais simplificado de organoide) para demonstrar que o Sars-CoV-2 gera danos ao sistema nervoso, mas não consegue se replicar e produzir novas cópias virais ali.
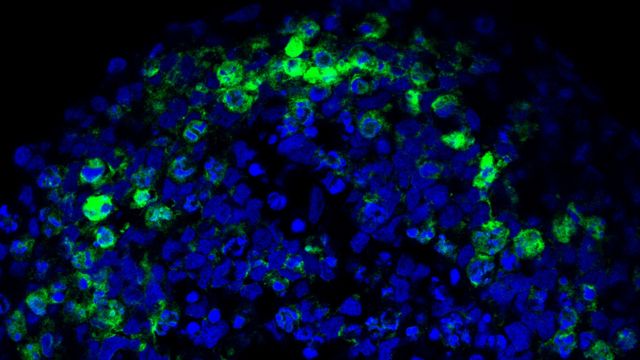
Já um trabalho feito na Unicamp avaliou a presença do coronavírus nos astrócitos, um tipo de célula do sistema nervoso. “A invasão viral parece modificar a forma como essas unidades produzem energia, o que impacta o funcionamento dos neurônios”, resume Souza.
Essa ação da covid-19 na massa cinzenta pode ser um caminho para explicar os sintomas neurológicos da doença, que chegam a acometer até 30% dos pacientes. Entre as manifestações mais comuns nesta região do corpo estão a perda ou o enfraquecimento de sentidos como olfato e paladar e o aparecimento de quadros de ansiedade e depressão.
Vale mencionar, no entanto, que essa é uma área em constante evolução. As pesquisas são realizadas neste exato momento e é possível que apareçam novidades num futuro próximo.
Os limites
Apesar de tantas vantagens, os organoides não são perfeitos e não permitem encontrar todas as respostas. “Essa é uma área que dá seus primeiros passos e enfrenta desafios importantes. Muitas dessas estruturas são feitas com células que ainda estão imaturas, o que significa que elas não são 100% comparáveis com os órgãos de um adulto”, avalia Núria Montserrat Pulido, professora do Instituto de Bioengenharia da Catalunha, na Espanha.
A bioquímica Shuibing Chen, da Universidade Cornell, nos Estados Unidos, destaca a grande variabilidade entre os modelos de miniórgãos usados pelos grupos de pesquisa. “É preciso padronizar esse material para entender as aplicações de nossos esforços no mundo real”, conta.
O investimento financeiro é outra barreira a ser considerada neste contexto. “Os materiais que usamos são caros e estamos trabalhando para criar sistemas custo-efetivos”, completa Chen.
Souza destaca mais um impeditivo: os miniórgãos (ainda) são estruturas isoladas, que não interagem com outros sistemas que compõem o corpo humano. Com isso, não é possível entender como os efeitos do coronavírus nos rins, por exemplo, repercutem no coração ou no intestino. “Quem sabe no futuro não tenhamos diferentes organoides conectados, de maneira que eles interajam no laboratório?”, vislumbra.
Se, em seus primeiros passos, os organoides já proporcionaram tanto conhecimento, imagine o que eles poderão fazer quando forem aperfeiçoados
Via BBC